
2025年1月15日,河南省科学院首席科学家、中科院生物物理所研究员姬广聚团队在Cell Metabolism (IF: 27.7)发表题为“Exosomal miR-302b rejuvenates aging mice by reversing the proliferative arrest of senescent cells”的研究论文,该研究从科学层面证明了细胞衰老可以被逆转的可能性,并提出了创新的“Senoreverse”逆转衰老策略。本文中单细胞转录组测序技术服务由北京百奥益康提供。

摘要
细胞衰老是衰老的一个标志,涉及细胞周期的稳定退出。衰老细胞(SnCs)与衰老和衰老相关疾病密切相关,使其成为抗衰老干预的潜在靶点。在这项研究中,我们证明了人类胚胎干细胞衍生的外泌体(hESC-Exos)通过恢复体外SnCs的增殖能力来逆转衰老。在衰老小鼠中,hESC-Exos治疗重塑了SnCs的增殖景观,导致了年轻化,这可以通过延长寿命、改善身体机能和减少衰老标志物来证明。Ago2 Clip-seq分析发现,在hESC-Exos中富集的miR-302b特异性靶向细胞周期抑制剂Cdkn1a和Ccng2。此外,在24个月的观察期内,miR-302b治疗逆转了体内SnCs的增殖停滞,导致返青而没有安全性问题。这些发现表明,外泌体miR-302b具有逆转细胞衰老的潜力,为减轻衰老相关病理和衰老提供了一种有希望的方法。
研究结果
首先,作者通过实验发现hESC-Exos可使衰老的IMR-90细胞恢复活力并重塑其增殖潜力。随后,为了观察hESC-Exos对与增殖相关的转录谱的影响,对通过FCM分选的SnCs进行了单细胞RNA-seq(scRNA-seq),共获得了16741个单细胞的转录组数据:Dox-PBS中的6311个和Dox-Exos中的10430个。通过绘制每个细胞群中G1/S相对于G2/M基因的平均表达来分析细胞周期进程,揭示完整的细胞周期轨迹。根据细胞的细胞周期进程对细胞进行分级,Dox-Exos在S期细胞的比例方面优于Dox-PBS,增加了约17%(图1D和1E)。
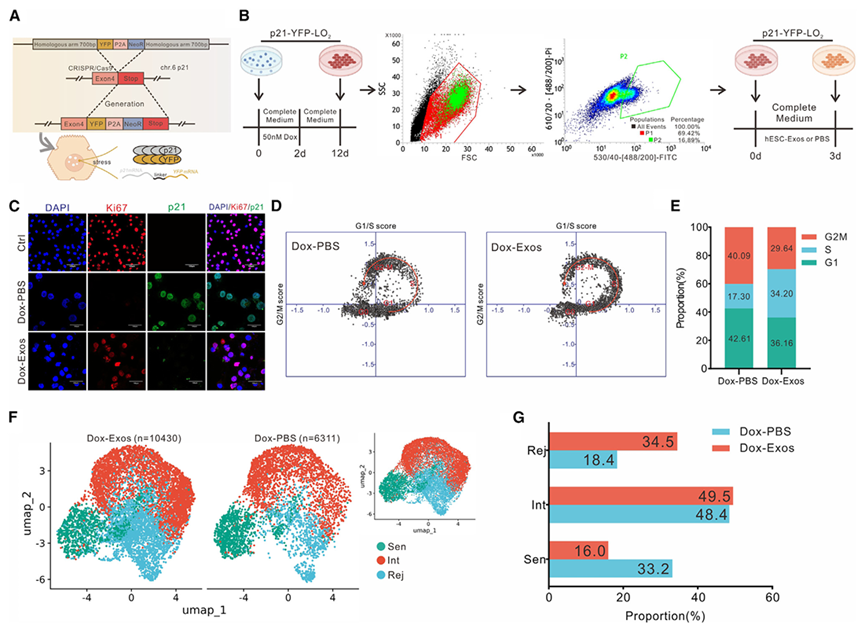
图1 hESC-Exos以单细胞分辨率逆转SnCs增殖停滞
根据先前报道的增殖和衰老marker对细胞群进行注释,将大量表达MKI67和PCNA的细胞定义为再生细胞(Rej),将大量表达CDNK1A和TP53的细胞定义为SnCs(Sen),将其他细胞定义为处于中间状态的细胞(Int)。热图分析揭示了三种高表达特定基因簇的细胞类型:Sen和PCNA中的S100P、CDKN1A和CDKN3,Rej中的MKI67和MCM5(图S1F)。Dox-PBS和Dox-Exos细胞表现出高水平的衰老(CDNK1A和TP53)和增殖(MKI67和PCNA)marker(图S1G)。UMAP分群图显示,与Dox-PBS相比,Dox-Exos具有更高的Rej细胞比例和更少的Sen细胞比例(图1F和1G)。
接下来,我们沿着从Int到Sen和Int到Rej的伪时间轨迹识别DEGs。模块1中的基因代表在Int向Rej分化期间上调的基因,包括CENPF、SERBP1和TOP2A,它们在有丝分裂期间富集。模块2包含在Int向Sen分化期间上调的基因,如CCNG2、CDKN1C和CDKN2A,它们参与细胞衰老和SASP的调节(图S1H)。总之,hESC-Exos治疗逆转了单个SnCs的增殖停滞,使它们能够恢复其增殖能力。
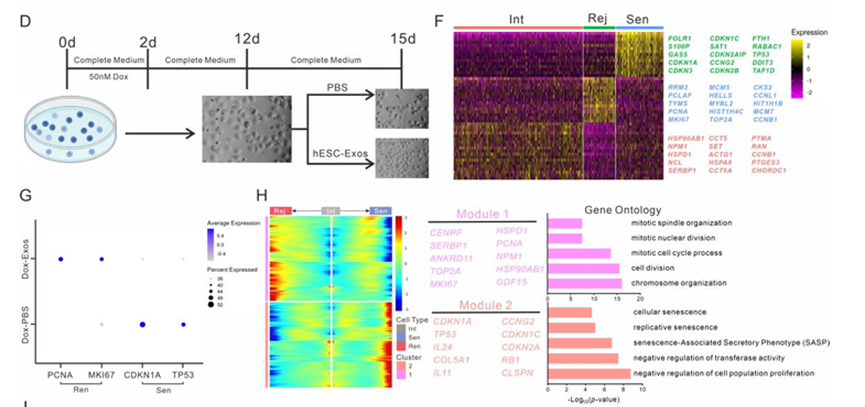
图S1 p21-YFPLO2细胞的hESC-Exos表征和scRNA-seq分析
作者通过小鼠模型评估了hESC-Exos的抗衰老效果,结果显示hESC-Exos处理使衰老小鼠的衰老表型逆转至更具活力的状态。接下来,作者研究了hESC-Exo处理对体内细胞增殖的影响。对分离自aging-Exos和aging-PBS小鼠(每组n=3)的肝脏和皮肤组织进行了scRNA-seq。然后将单细胞转录组数据与之前报道的从3个月大的C57BL/6J雄性小鼠(设定为年轻组)中分离的肝脏和皮肤组织的测序数据进行整合。共确定了肝脏中的28个细胞群和皮肤中的25个细胞群。根据标准细胞类型特异性marker来确定细胞类型(图S2A-S2D)。然后,基于Mki67表达提取有丝分裂细胞的scRNA转录组数据,并分析肝脏和皮肤组织中这些细胞的细胞周期阶段。衰老减少了肝脏和皮肤组织中S期细胞的比例,这种情况可通过hESC-Exos治疗逆转(图2A)。然后将DEGs与从PathCards数据库中检索的调节细胞周期途径的基因重叠,共享的子集被称为中枢细胞周期相关基因(CCGs)。鉴定了aging-PBS和年轻小鼠之间以及aging-PBS和aging-Exos小鼠之间的CCGs,并分别称为“aging CCGs”和“Exos CCGs”。agingCCGs和Exos CCGs之间的共享基因被鉴定为恢复CCGs(图2B)。值得注意的是,在肝脏和皮肤组织中交集中显著出现了10个恢复CCGs,包括4个下调的恢复CCGs(Cdkn2a、Cdkn1a、Cdkn1b和Ccng2)及6个上调的恢复CCGs(E2f1、Mki67、Top2a、Cdk1、Ccnb1和Pcna)。(图2C)。
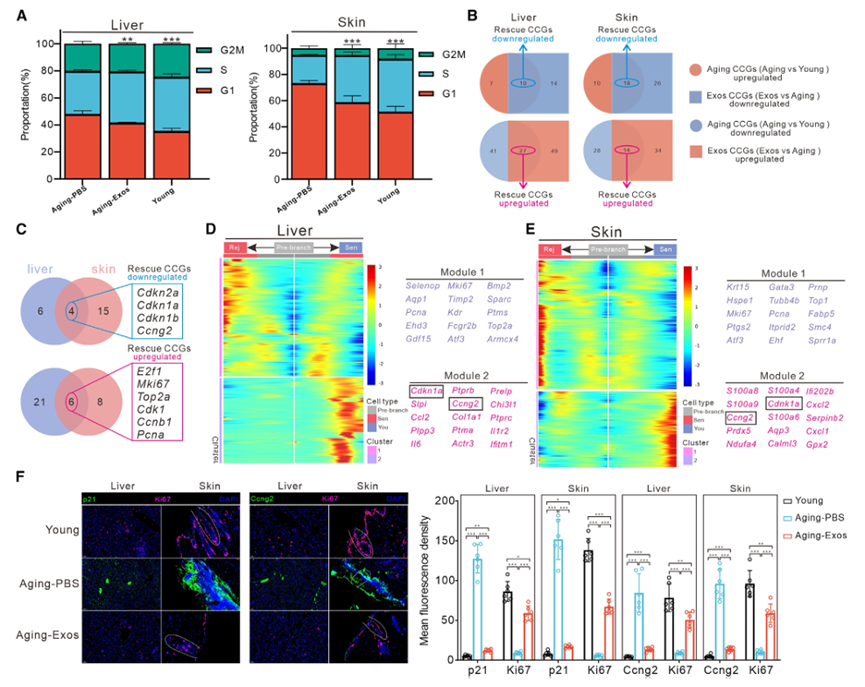
图2 hESC-Exos治疗重塑了衰老小鼠的增殖过程
接下来,我们基于Mki67表达提取有丝分裂细胞的scRNA转录组数据。在UMAP降维聚类后,细胞簇被分为Rej细胞(Mki67的高表达和Cdkn1a的低表达)、Sen细胞(Cdkn1a的高表达和Mki67的低表达)和Int细胞(Cdkn1a和Mki67的中等表达水平)(图S2E和S2F)。伪时间轨迹分析揭示了驱动从Sen到Rej细胞状态转变的关键因素(图2D、2E和S2G–S2I)。在肝组织中,模块1包含Sen-Rej转化过程中上调的基因,如Selenop、Pcna、Mki67和Top2a,而模块2包含Sen-Rej分化过程中下调的基因,包括Cdkn1a、Ccl2、Ptprb和Ccng2(图2D)。在皮肤组织中,模块1包含在Sen-to-Rej分化期间上调的基因,包括Krt15、Mki67、Atf3和Fabp5。相比之下,模块2基因代表在Sen-to-Rej分化过程中下调的基因,包括S100a8、S100a9、Ccng2和Cdkn1a(图2E)。
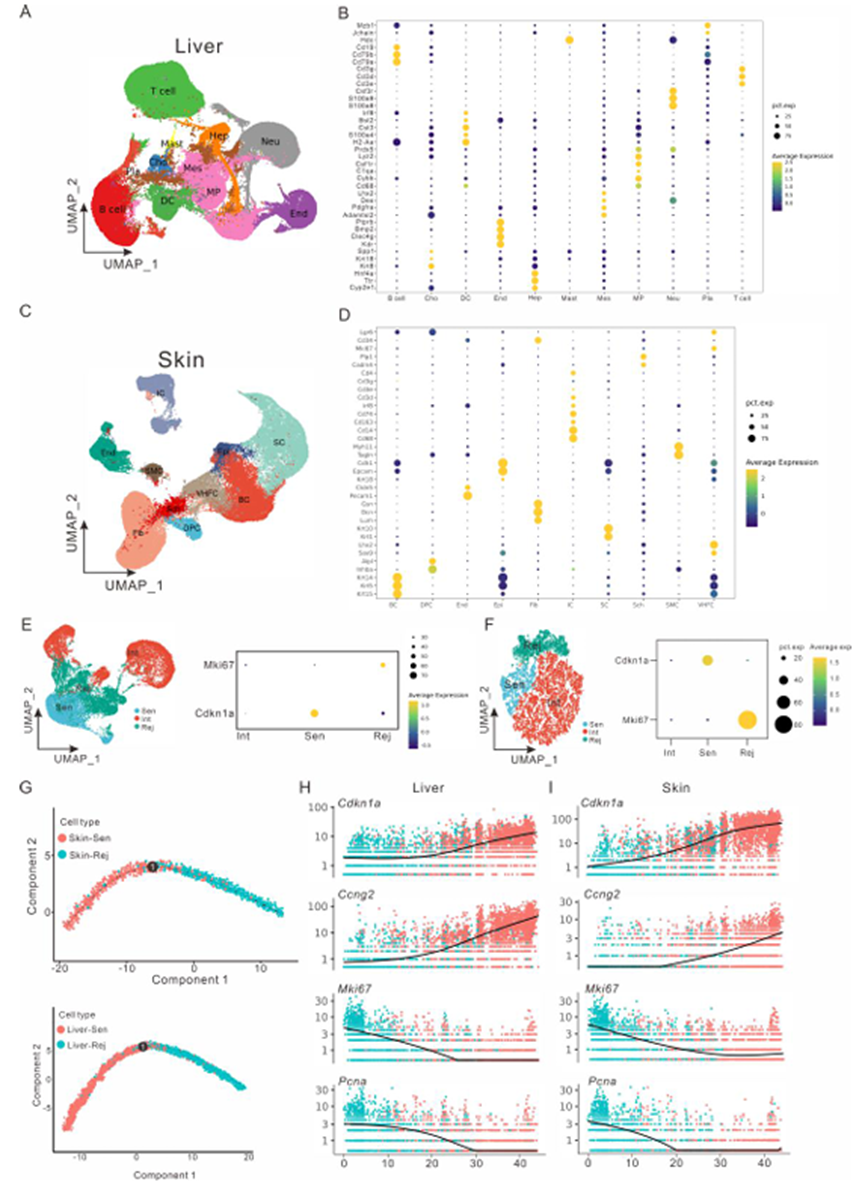
图S2 肝脏和皮肤组织中细胞类型的鉴定和关键细胞类型的组成变化
在这里,我们重点关注在伪时间轨迹推断中发现的共享基因Cdnk1a和Ccng2(也称为恢复CCGs),它们有助于肝脏和皮肤组织中的细胞衰老。免疫荧光染色进一步证实,hESC-Exos治疗抑制了老化肝脏和皮肤中Cdkn1a和Ccng2的表达(图2F)。总的来说,Cdkn1a和Ccng2是促进细胞周期停滞和促进衰老的重要因素。hESC-Exos治疗逆转了SnCs的细胞周期停滞,从而通过抑制Cdkn1a和Ccng2的表达来促进再生。这些数据表明,hESC-Exos治疗部分恢复了衰老小鼠的增殖相关信号。
hESC-Exos包含一系列与衰老过程相关的生物活性物质,其中就包括miR-302b,能够精准靶向抑制细胞周期关键抑制因子Cdkn1a和Ccng2,从而在体外恢复衰老细胞的增殖能力。对衰老小鼠模型持续递送miR-302b不仅显著减缓了衰老引起的体重下降,还延长了中位寿命和最高寿命,显著降低了死亡风险。综合来看,长期递送miR-302b能够显著延长寿命、改善衰老表型,同时未提升肿瘤和其他疾病的发生率。
研究结论
综上所述,本研究首次提出了“Senoreverse”策略,在不改变衰老细胞固有属性的前提下,通过帮助其摆脱“时间枷锁”、重启增殖周期,实现了细胞和机体的衰老逆转。在这一创新性策略的指导下,研究团队从 hESC-Exos 中成功筛选并验证了 miR-302b 作为候选“Senoreverse”核酸药物的有效性和安全性。miR-302b 能够精准解除衰老细胞的增殖停滞,显著延长动物寿命,改善衰老表型,并有效降低慢性炎症,同时未引发安全隐患。这一研究不仅从理论和实践层面验证了“Senoreverse”策略的可行性,还为衰老相关疾病的治疗提供了全新的方向和解决方案。
参考文献:
Bi Y, Qiao X, Cai Z, et al. Exosomal miR-302b rejuvenates aging mice by reversing the proliferative arrest of senescent cells. Cell Metab. 2025 Jan 13:S1550-4131(24)00481-9. doi: 10.1016/j.cmet.2024.11.013.